KVALITAN - virtuálne chemické lagoratóriumStriebro / Dôkazy / Katióny I. triedy / Katióny / Teória
Dôkazy striebra
p-Dimetylaminobenzylidénrodanín
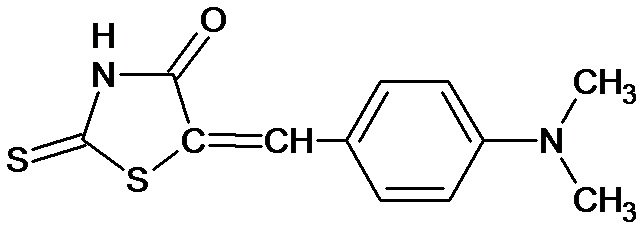
poskytuje s katiónom striebra v slabo kyslom prostredí červenofialovú zrazeninu. Túto reakciu možno výhodne použiť aj ako kvapkovú skúšku na striebro.
Za prítomnosti ortuti pridávame KCN, pričom vzniká K[Ag(CN)2] a málo disociovaný Hg(CN)2 ktorý s činidlom nereaguje. KCN pridávame aj v prítomnosti Au a Pt.
V prítomnosti Cu a Hg pridávame KCN, ale potom musíme pridať ešte HCl na rozrušenie meďného komplexu, ktorý reaguje s činidlom.
Ditizón
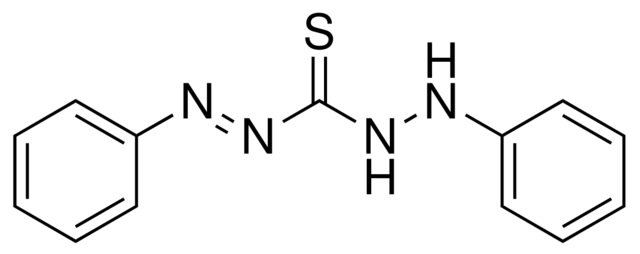
neutrálne alebo slabo zásadité roztoky solí strieborných s ditizónom poskytujú červenofialovú, vločkovitú, v CCl4 nerozpustnú zrazeninu . Naproti tomu kyslé roztoky solí strieborných poskytujú žltú zrazeninu, ktorá trepaním s CCl4 prejde do vrstvy CCl4. Túto metódu možno použiť na dokazovanie striebra v prítomnosti všetkých katiónov, ktoré s týmto činidlom reagujú, a v prítomnosti ostatných katiónov, keď ich maskujeme.
Tionalid
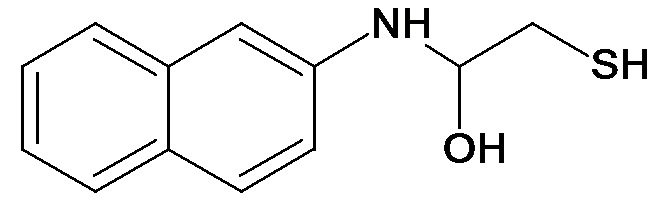
vylučuje z roztokov strieborných solí mierne okyslených kyselinou dusičnou, žltú zrazeninu. Túto metódu možno použiť aj na oddeľovanie striebra od olova a tália.
Ako činidlo sa pripravuje 1 % roztok tionalidu v alkohole alebo kyseline octovej.
Propyléndiamín
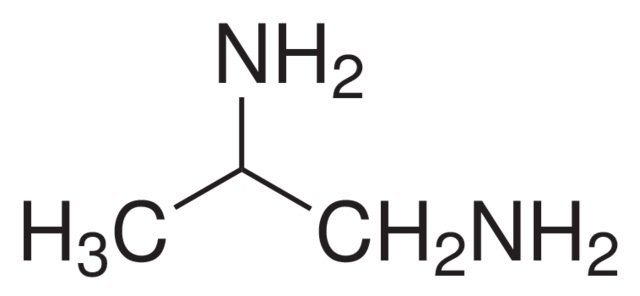
a síran meďnatý CuSO4. 5 H2O tvorí vo vodnom roztoku komplexný katión, ktorý zráža strieborné soli v podobe komplexnej zlúčeniny bledofialovej farby. Roztoky solí striebra musia byť neutrálne alebo slabo amoniakálne. K roztoku pridáme najprv jodid draselný a vzniknutý jodid strieborný rozpustíme v nadbytku KI, potom roztok zahrejeme až do varu a pridáme k nemu čerstvo pripravený koncentrovaný roztok činidla. V prítomnosti väčšieho množstva striebra sa vylúčia hneď a zo zriedených roztokov až po vychladnutí fialové kryštáliky.
Ako činidlo sa používa vodný roztok pripravený rozpustením vzorcovej váhy CuSO4. 5 H2O a 2 grammolekúl propyléndiamínu v práve potrebnom množstve vody.
Bromid draselný
Na filtračný papier nanesieme kvapku skúmaného roztoku a obkreslíme ju ceruzkou. Papier osušíme a vložíme na dve minúty do roztoku bromidu draselného. Potom ho umyjeme destilovanou vodou a vložíme do roztoku metolu. Prítomné striebro sa vyredukuje v kovovej forme ako tmavá škvrna, ktorej veľkosť sa riadi podľa množstva prítomného striebra.
Ako činidlo sa používa 0,02 mol l-1 bromid draselný a roztok 10 g metolu a 50 g kyseliny citrónovej v 500 ml destilovanej vody.
Síran ceričito-amónny alebo dusičnan ceričito-amónny
Žltý roztok soli ceričitej sa za prítomnosti AgCl odfarbí, lebo soľ ceričitá sa redukuje na soľ ceritú. Na platničku alebo do malej misky dáme dve kvapky činidla a kvapku skúmaného roztoku mierne' okysleného kyselinou dusičnou. V prítomnosti striebra sa roztok odfarbí. Vzhľadom na to, že roztok sa môže odfarbiť aj za neprítomnosti striebra, musíme robiť súčasne aj slepý pokus. Ako činidlo sa používa 10% roztok síranu v 10 mol l-1 HCl alebo 0,25% roztok dusičnanu ciničito-amónneho v 1 % kyseline dusičnej.
Síran manganatý
Účinkom síranu mangánatého v prítomnosti manganistanu draselného v prostredí kyseliny chlorovodíkovej. Prítomnosť striebra katalyzuje reakciu medzi dvojmocným a sedemmocným. mangánom, pričom vzniká tmavá zrazenina štvormocného mangánu, ktorá prejde na bezfarebnú zlúčeninu dvojmocného mangánu. Pri dokazovaní striebra postupujeme takto: Na dno malého téglika pridáme dve kvapky činidla, kvapku skúmaného roztoku a trocha kyseliny soľnej. V prítomnosti striebra sa čierna zrazenina odfarbí.
Potrebné roztoky: 0,1 % vodný roztok síranu mangánatého,0,1 mol l-1 manganistan draselný a 10 mol l-1 kyselina chlorovodíková. Činidlo sa pripravuje pred použitím zmiešaním po jednej kvapke z každého roztoku.
Chlorid rubídny
Účinkom chloridu rubídneho sa z roztoku vylučuje bezfarebná zrazenina zloženia Rb[AgCl2]. Dôkaz sa robí nasledujúcim postupom: Na podložné skielko dáme kvapku mierne kyslého skúmaného roztoku a do nej vložíme kryštálik chloridu rubídneho a zmes opatrne zahrejeme nad mikroplameňom. Ak vzniknú bezfarebné ihličky, je to dôkazom prítomnosti striebra. Ako činidlo používame nasýtený roztok chloridu rubídneho.



